- 近期网站停站换新具体说明
- 按以上说明时间,延期一周至网站时间26-27左右。具体实施前两天会在此提前通知具体实施时间
主题:NgAgo曲终人未散,江上数峰青 -- 陈王奋起
2016年5月2日,《自然》杂志子刊《自然·生物技术》刊登了一篇名为《DNA引导的NgAgo蛋白可用作基因编辑工具》的文章,作者为河北科技大学韩春雨团队,这是NgAgo首次被提出。文章称,NgAgo能在向导DNA的指引下,对目标基因有效切割,可用于对人类细胞的基因编辑。
这篇文章发表后,在种种外界因素的推动下,随即在国内引发轰动效应,某些国内专家和媒体称之为“诺奖级”的发现。同时,NgAgo被视为新的基因编辑技术,可比肩目前世界上应用最广泛的基因编辑工具CRISPR/Cas9。
基因编辑,指人为对DNA片段进行有目的的改造,包括插入、敲除基因等操作,使其序列发生变化。基因编辑和电脑上编辑一份文档类似,只不过,其操作对象是直接影响生物体特质的终极密码——DNA。通常,基因编辑分为剪开与修复两个步骤。因此,要想进行基因编辑,首先要有把好“剪刀”。
目前,科学家们用得最顺手的基因剪刀就是CRISPR/Cas9,其开发者是美国麻省理工学院华裔科学家张锋和加州大学伯克利分校教授詹妮弗·杜德娜等(顺便八卦一下,张峰和杜德娜争夺CRISPR的专利所有权,张锋申请晚几个月,但凭借更早的实验室记录本最后赢得胜利,获得专利授权)。
实际上,CRISPR/Cas9最初是细菌抵御外敌的防御系统:当有病毒或外来DNA首次入侵时,CRISPR/Cas9就会剪切一段带有入侵者身份特质的DNA(核糖核酸),将其记录在案,等外敌再次来犯时,CRISPR/Cas9会依据之前记录的DNA信息,转录出一段起着向导作用的RNA,指引自己对来敌精准识别,准确打击。就是这样一套系统,被科学家们用作基因编辑的工具。
但CRISPR/Cas9也有缺点:其剪切点一定要位于一段处于特定位置、名为PAM序列的上游,这意味着CRISPR/Cas9的工作范围并不能无死角、全覆盖。而引导其剪切的RNA还有着容易变身的特点,这同样会影响到剪切的准确度。因此,研发更可靠、更准确的新剪刀成了科学家们的目标。这一背景下,名为Argonaute(简称Ago)的蛋白家族开始相继登场。
与CRISPR/Cas9相似,Ago蛋白同样是生物体的防御系统。最初,人们发现,真核生物体内的Ago蛋白能降解外来的RNA,进而又发现,来源于原核生物的Ago蛋白可以消灭入侵的DNA。从形态上来说,原核与真核生物的区别在于细胞核有没有核膜,原核生物是指一类细胞核无核膜包裹的原始单细胞生物,真核生物则涵盖了包括人类在内的所有动植物等生命体。
2014年,荷兰瓦赫宁根大学教授约翰·范德欧斯特在原核生物的Ago蛋白家族中,发现一种名为TtAgo的蛋白能与具有向导作用的DNA结合,在65°C条件下,切割目的DNA。但显然,高温限制了其发挥更大作用的潜力。
业界一度认为,韩春雨的研究突破性地解决了这一弊端。通过对比筛选,他发现另一种来源于格氏嗜盐碱杆菌的Ago蛋白,并将其命名为NgAgo。通过实验证实,这种蛋白能在37°C常温下,结合向导DNA,实现基因编辑。这意味着NgAgo在人类疾病治疗、生物制药等领域将有广阔的应用前景。而相比CRISPR/Cas9,NgAgo还有着不特定依赖于PAM序列、以DNA 为向导不易失效和脱靶、容错率低、效率高等一系列优点。
2016年5月8日,新媒体平台“知识分子”,以《韩春雨:“一鸣惊人”的中国科学家发明世界一流新技术》为题,报道了韩春雨其人与他的研究。“知识分子”在这篇注明为“特稿”的文章前加了一段编者按,其中写道:“令国人激动的是,韩春雨在河北科技大学条件不好、经费缺乏、人员很少的情况下做出的研究,优于世界一流的麻省理工、哈佛、斯坦福。《知识分子》主编、北京大学教授饶毅将韩春雨推介给编辑部,在此我们特别刊出专访,以飨读者。”
此后,国内媒体蜂拥而上,对韩春雨的研究成果进行报道。韩春雨先后被评为河北省科协副主席、河北省最美教师、国家“中青年科技创新领军人才”候选人、“长江学者奖励计划”候选人、2016年度高校享受政府特殊津贴人员等。2016年8月,河北省发改委还批复并“原则同意”了估算总额达2.24亿元的河北科技大学基因编辑技术研究中心的工程建设项目。
质疑声与赞誉几乎同时而至。在其论文发表后不到20天,现任美国普林斯顿大学分子生物学系教授、当时在清华大学任教的结构生物学家颜宁在微博上首次提出韩春雨论文结果的可重复性存在问题。此后,类似质疑在未名空间、知乎、百度贴吧,西西河等论坛上出现。
至2016年9月,当时一力推荐的饶毅与中科院院士邵峰联名致信河北科技大学校长,称“宜谨慎对待韩春雨及其研究成果”,并建议成立专家委员会,核实韩春雨研究成果。当年10月,北大生科院教授魏文胜等13名国内生物学家联名在媒体上公开发声,表示无法重复该实验结果,希望韩春雨公开所有原始数据,呼吁学校及相关方介入调查。
2016年11月,《自然·生物技术》编辑部表示,正在调查该论文。之后,韩春雨给《自然·生物技术》编辑部补充了相关实验数据。2017年1月,国家知识产权局撤回了韩春雨团队以Ago为核心的基因编辑技术专利。据介绍,目前,该团队以国际专利形式重新提交申请,并处于公开状态。同年8月,由于一直没有重复出实验结果,韩春雨团队撤回论文。《自然·生物技术》编辑部发表了《是该数据说话的时候了》的社论称,“我们现在确信韩春雨的撤稿决定是维护已发表科研记录完整性的最好做法。”
之后,韩春雨团队继续寻找论文结果不能重复的原因。时隔一年后,河北科技大学发文称,韩春雨团队不存在主观造假。但依据有关规定,取消韩春雨所获得的荣誉称号,终止韩春雨团队承担的科研项目并收回科研经费。韩春雨团队回应说,实验设计存在缺陷、研究过程存在着不严谨的问题。
有意思的是,学术界并没有因为韩春雨撤回他的论文就彻底放弃NgAgo。2019年4月4日,美国冷泉港实验室运营的网站bioRxiv发表论文称,普渡大学的科研人员发现了一种名为论文,题为《NgAgo的蛋白能切割DNA(脱氧核糖核酸)》,称NgAgo可以提高大肠杆菌体内基因同源重组的效率。bioRxiv是免费向生物学家开放的预印本文献库,也就是说,发表在上面的文章都是尚未获得同行评议的作者原始文稿。我在Google上查了一下,到今天还不是正式发表状态。
在基因编辑过程中,同源重组被视为细胞常用的修复手段,基因剪刀断开DNA链条的行为,会刺激同源重组的发生,如果再提供外源供体,则能完成DNA序列的交换。几个月前,华中农业大学农业微生物国家重点实验室的研究团队也在国际期刊《核酸研究》上发文,同样称NgAgo能促进几种细菌体内的基因同源重组,可视为潜在的基因编辑工具。
虽然“韩春雨事件”告一段落,但由他首先提出的NgAgo能否作为基因编辑工具仍无定论。
早在2016年11月,南通大学神经再生重点实验室副教授刘东与复旦大学生命科学学院研究员王永明在《自然》杂志子刊《细胞研究》上发表了国内第二篇关于NgAgo的文章。文章称,用NgAgo可以“敲低”斑马鱼基因,导致其眼部发育缺陷。但由于“敲低”只是使基因表达降低,并没有改变基因序列,因此,谈不上“编辑”。而由于研究对象不同,刘东等人称,其研究也“不能对此前韩春雨的结论证实或证伪”。
相比之下,最近发表的几项关于NgAgo的新研究似乎带给人们更多希望。
在美国普渡大学的研究中,NgAgo首先被证实在体外实验中具有切割DNA的能力。
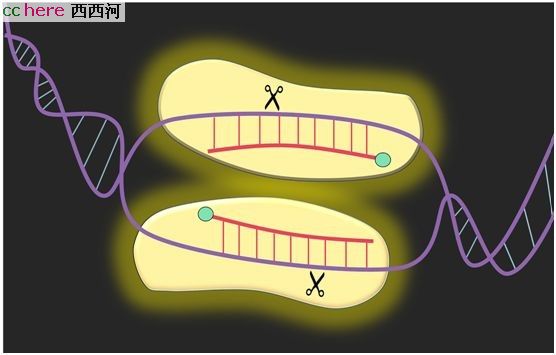
图片来自Kevin Solomon/Purdue University。
更进一步,研究人员发现,NgAgo上两个名为PIWI和RepA的部位都能独立切割DNA。但与韩春雨结论不同的是,在普渡大学开展的体外实验中,NgAgo切割时,并没有和本该配对的向导DNA结合。负责这项研究的普渡大学农业与生物工程助理教授凯文·所罗门在接受《中国新闻周刊》采访时推测说,这有可能是NgAgo事先已结合了DNA在复制过程产生的其他碎片DNA片段,充当向导。
而在大肠杆菌的体内实验中,NgAgo被证明能结合向导DNA,并依靠其切割能力,提升大肠杆菌同源重组的效率。今年2019年1月,华中农业大学的研究同样证明:在巴氏杆菌和大肠杆菌体内,NgAgo能提升基因同源重组的效率。但与普渡大学和韩春雨的研究不同,该论文作者华中农大动物科学技术学院、农业微生物国家重点实验室教授张安定、金梅林等人观察到,NgAgo对同源重组的促进,是通过NgAgo的PIWI部位与一种助力同源重组的酶RecA的相互作用。“当然,我们不排除它两种原理都在起作用。”张安定在接受《中国新闻周刊》采访时说。
但需要注意的是,无论是华中农大还是普渡大学的研究,目前都聚焦的是NgAgo在原核生物中的切割作用。“我们并没有打算重复韩春雨论文中的研究结论,也就是在哺乳动物细胞中进行基因编辑。”所罗门说,“现在说NgAgo能否适用于人类细胞基因编辑为时尚早,我们能够说的是,这是又一个能提升细菌中基因编辑的工具,对生物燃料的生产、制药等方面能发挥作用。”
事实上,在韩春雨论文结果发表之初,国内也曾一度掀起跟风研究热潮。据某不愿具名的业内人士称,国内六七家在这一领域较有实力的科研机构此前都对NgAgo很感兴趣。但在韩春雨论文被热烈追捧又遭到强烈质疑后,这些研究者又逐渐退出,基本不再涉足该研究领域。相比之下,在世界范围内,对于NgAgo乃至更大范围的Ago蛋白家族的研究,仍进展不断。
2019年2月,加州理工学院生物工程系教授阿列克谢·阿拉温在bioRxiv上发表论文称,源于丁酸梭菌的CbAgo具有高活性,可用于在中等温度下切割单链和双链DNA。阿拉温进一步表示,在37℃条件下,CbAgo可能在真核细胞中具有活性。前文提到的荷兰瓦赫宁根大学教授范德欧斯特近期也在bioRxiv发表了类似的研究成果。不过,他对《中国新闻周刊》回复称,“迄今为止,我们还没有用CbAgo进行人类细胞基因组的编辑,如果应用,还需要更多的优化”。
2019年7月30日,中科院动物研究所王皓毅团队和中科院北京生命科学研究院赵方庆团队合作,在 Cell Discovery 杂志发表了题为:Argonaute proteins from human gastrointestinal bacteria catalyze DNA-guided cleavage of single- and double-stranded DNA at 37 °C 的研究论文。该论文发现了来自人类胃肠道细菌的两种Ago蛋白(CpAgo、IbAgo)可在37℃下在DNA引导下实现对DNA单链和双链的切割。而CpAgo和IbAgo,也是韩春雨发现的NgAgo的近亲。
来源:https://www.nature.com/articles/s41421-019-0105-y
国内某权威科研院所一名长期研究Ago蛋白家族的研究人员称,当初,韩春雨的研究只是该领域众多科研成果中的一项,即使文章结论成立,也并无特别值得关注之处(此处有山西醋1斤,注意规避)。他的研究之所以引发轰动效应,主要是媒体的炒作。在她看来,眼下,Ago蛋白用作基因编辑工具还不太合适,“就像拿一把非常钝的刀子去切肉一样”,“但不排除以后大家想到什么样的办法对蛋白进行一个非常大的改造,或者两三个蛋白一起作用,研究人员应该想一些更加有用的办法。一旦基础研究有了突破,应用上的突破也会很快跟上。那么究竟突破在哪里?我觉得还得给大家更多时间。”
前述不愿具名的业内人士则表示,从目前国内外最新的研究成果来看,NgAgo有其科研价值,“显现出来很多的效果都是值得我们去研究的”。他认为,相较国外的持续跟进,如果国内因为韩春雨当年被“捧杀”而不再关注这一研究,将在这一领域处于落后被动的地位。
- 相关回复 上下关系3
🙂NgAgo曲终人未散,江上数峰青
🙂待认可未通过。偏要看
🙂陈王啥时能谈谈颜宁和施一公呢? 审度 字0 2020-01-31 12:59:58